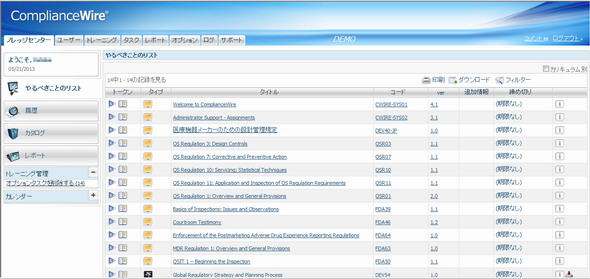
医療機器のFDA対応を効率化――UL JapanがFDA査察対応サービス:ビジネスニュース
UL Japanが、FDA(米国食品医薬品局)の査察/規制順守に対応するためのコンプライアンスソリューションサービス「ComplianceWire」を国内で販売。オンラインによる効率的なトレーニングで、FDAの厳しい査察に対応。
第三者製品安全認証機関である米ULの日本法人、UL Japanは2013年7月25日、FDA(米国食品医薬品局)の査察および規制順守に対応するためのコンプライアンスソリューションサービス「ComplianceWire」の国内販売を開始すると発表した。
同サービスは医療機器・医薬品関連企業におけるFDA申請後のコンプライアンスの維持・管理を目的として開発されたもの。日本から米国へ医療機器や医薬品を輸出する際には、FDAへの届け出・承認申請が必要となる他、FDAの定期的な査察(品質の検証)に対応していかなくてはいけない。
「FDAの査察では、コンプライアンスに順守しているかが厳しくチェックされる。この査察に企業が効率的に対応できるように、オンライントレーニングの形式で提供するのが本サービス。これまで米国で実施していたものを、今回、日本向けにカスタマイズした」(UL Japan)。
450種類のトレーニングコースのうち、110コースがFDAとの共同監修で作成されている。トレーニングの内容は初級から中級者向けが中心となっており、幅広く基礎的なトレーニングが習得できるという。
また、米国連邦規則「電子記録・電子署名に関する規則」(21 CFR Part 11)に適合しており、医療機器・医療品関連企業の製造部門だけでなく、品質管理やCSR、コンプライアンスなどを担当される部門など、幅広く社内外で利用できるという。
「ComplianceWireは、13年ほど前に規制当局側のFDA査察官向けのトレーニングプログラムとして開発したのが始まり。それまで座学でやってきたものをオンライントレーニングへ移行し、査察官のトレーニングプログラム自体が非常に効率化できたことから、その有効性には定評がある。オンラインサービスで基礎をしっかりトレーニングしてから実地に臨むことで、厳しいFDAの査察にも効率的に対応できる」(UL Japan)。
Copyright © ITmedia, Inc. All Rights Reserved.
関連記事
 認証機関からビジネスパートナーへ、UL Japanが新戦略
認証機関からビジネスパートナーへ、UL Japanが新戦略
UL Japanは、これまでの「第三者認証機関」という位置付けから、エネルギー関連技術や日本が先行する材料技術などの先端技術分野にフォーカスしつつ、顧客が国際競争力を高めるための「ビジネスパートナー」へと事業の方向性をシフトしていく。- スマートグリッドが今年のキーワード、UL Japanが事業戦略を明らかに