リチウム-空気電池の過電圧を“水”が低減:EV搭載が期待される次世代電池の効率を改善
産業技術総合研究所(産総研)は複数の大学と共同で、触媒としてわずかに水を添加した有機電解液DMSOを用いると、リチウム-空気電池の空気極の過電圧を大幅に低減できると発表した。
産業技術総合研究所(産総研)省エネルギー研究部門の周豪慎首席研究員は2015年7月、複数の大学と共同研究を行い、触媒としてわずかに水を添加した有機電解液DMSOを用いると、リチウム-空気電池の空気極の過電圧を大幅に低減できると発表した。
空気極に炭素・ルテニウム・二酸化マンガンを用い、有機電解液DMSOに対して約100ppmの水を加えると、充電過電圧が約0.21Vまで縮小したという。
過電圧でカーボンや触媒が腐食
リチウム-空気電池は空気中の酸素(O2)を電気化学反応に利用している。放電する場合は、外部回路からの電子と、電解液中のリチウムイオン(Li+)が、空気極中に拡散してきた酸素と還元反応を起こして、過酸化リチウム(Li2O2)になる。充電する場合は、逆に(Li2O2)が酸素発生反応を伴って分解し、リチウムイオンと酸素になるのが理想的だ。
しかし、空気極の(Li2O2)酸素発生反応の過電圧が1.0V以上の大きな値になってしまい、その高い過電圧によって空気極に用いられているカーボンや触媒なども腐食されてしまう。そのため、腐食対策として、カーボンフリーの空気極、過電圧対策として、ヨウ素イオンなどの利用が盛んに研究されている。
有機電解液DMSOに触媒としてわずかな水を加える
今回の測定システムは、空気極の過電圧を評価するために、負極にリン酸鉄リチウム(LiFePO4)を用い、DMSOに対して約100ppmの水を加えた有機電解液とし、空気極の触媒には、炭素とルテニウム(Ru)と二酸化マンガン(MnO2)を用いている。
この構成の電池は、空気極の上に放電で生成したLi2O2がH2Oと反応して、固体状の水酸化リチウム(LiOH)と過酸化水素(H2O2)になる(Li2O2+2H2O=2LiOH+H2O2)。LiOHは低い電位で、酸素発生反応により分解され、Li+、O2とH2Oになり、また、H2O2もMnO2触媒による酸化還元反応で、O2とH2Oになる。これらの反応で、H2Oは、中間体LiOHを経由して消耗せずに循環して触媒の役割を果たしている。
今回の空気極により、空気極のカーボン+Ru+MnO2の重さを基準にした電流密度250mA/gで、充電と放電の過電圧がそれぞれ、0.21Vと0.11Vに低減されたという。電流密度が500mA/gと1000mA/gの場合も、充電の過電圧が大幅に削減されている。
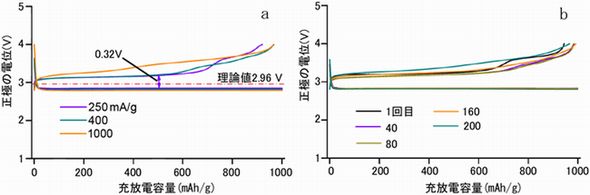 リチウム-空気電池用空気極のレート特性(左)/電流密度500mA/g(=0.25mA/cm2)における充放電サイクル試験では、安定した200回の充放電サイクル特性が得られた(右) (クリックで拡大)出典:産総研
リチウム-空気電池用空気極のレート特性(左)/電流密度500mA/g(=0.25mA/cm2)における充放電サイクル試験では、安定した200回の充放電サイクル特性が得られた(右) (クリックで拡大)出典:産総研電気自動車がより長距離走行できる電池として注目
リチウム-空気電池は、理論的にリチウムイオン電池の約5〜8倍の重量エネルギー密度をもつ。電気自動車に搭載して、より長距離走行が可能になる高性能蓄電池として注目され、産総研は精力的に研究を続けている。
充電時の過電圧をはじめ、空気極での充電・放電の反応機構がよく分からないことや充放電サイクル特性が悪いなどの課題があるが、空気極の構成の最適化や、作動環境の検討などを行い、性能の優れたリチウム-空気電池の開発を目指すとしている。
関連記事
 赤い微生物「ジオバクター」の燃料電池、廃水処理システムを変える?
赤い微生物「ジオバクター」の燃料電池、廃水処理システムを変える?
赤い微生物「ジオバクター」を使用した燃料電池(MFC:Microbial Fuel Cell)による廃水処理技術の開発が進んでいる。廃水中にふくまれる有機物を、電気に変換しながら分解することで、大幅な省エネを実現する上に、汚泥の発生も最小限にする仕組みだ。2015年6月5日〜6日に行われた「東大駒場リサーチキャンパス」において、同技術の取り組みについて聞いた。 容量がリチウムイオン電池の7倍!? 酸化物イオンを使う新原理の二次電池
容量がリチウムイオン電池の7倍!? 酸化物イオンを使う新原理の二次電池
東京大学大学院工学研究科教授の水野哲孝氏のグループと日本触媒は、現行のリチウムイオン電池の7倍に達するエネルギー密度を可能とする、新原理の二次電池の動作を実証したと発表した。この新原理の二次電池は、正極中における酸化物イオンと過酸化物イオンの酸化還元反応を利用する。 ニッケル亜鉛電池がニッケル水素電池を置き換える!? 日本触媒が新材料を開発
ニッケル亜鉛電池がニッケル水素電池を置き換える!? 日本触媒が新材料を開発
日本触媒は、「第5回国際二次電池展」において、ニッケル亜鉛電池の負極材料として利用できる新開発のアニオン伝導層一体型亜鉛電極を展示した。ニッケル亜鉛電池の最大の課題だった亜鉛電極上でのデンドライトの成長を抑制し、サイクル寿命を大幅に伸ばせることを特徴としている。 燃料電池車に再び熱い視線、大手自動車メーカーが次々協業
燃料電池車に再び熱い視線、大手自動車メーカーが次々協業
2013年7月、General Motorsとホンダが燃料電池車の共同開発を発表した。その半年前となる1月には、日産、ダイムラー、フォードも燃料電池車の開発で協業すると発表している。今後ますます厳しくなる自動車の排出ガス基準に対応すべく、燃料電池車への注目が再び高まっている。
Copyright © ITmedia, Inc. All Rights Reserved.
記事ランキング
- 「世界初」成果で1000層超3Dフラッシュに道筋、キオクシアとSandisk
- ナフサ危機で迫る「レジスト供給途絶」――世界の半導体工場を停止させる、もう一つの臨界点
- 次世代パワー半導体 「期待の5材料」の現在地
- パワー半導体世界市場、2035年は7兆円超え 酸化ガリウムも一定規模に
- 入学した瞬間終わったわ――「講義が英語」なんて一言も聞いてない!
- TSMCが次世代ロードマップ公表 A13/A12を29年投入へ
- SK hynixの四半期決算、驚異の売上高営業利益率70%超え
- 「データの死蔵に耐えられないエンジニア」がたどり着いたMASの沼
- TED、25年度は減収減益 「各事業磨き上げる」と新社長
- 村田製作所、25年度は売上高が過去最高 データセンター向けは70%増
